
生物医学新技术的浪潮正以前所未有的速度重塑人类健康的未来,从基因编辑、细胞治疗到合成生物学,这些前沿技术蕴含着治愈重大疾病的巨大潜力,同时也伴随着复杂的伦理挑战、不确定的生物安全风险与严峻的监管合规问题。在此背景下,《生物医学新技术临床研究和临床转化应用管理条例》(以下简称《条例》)的颁布,标志着中国在生命科学领域的法治化治理迈出了至关重要的一步。作为我国首部专门针对生物医学新技术从“实验室研究”迈向“临床转化”全链条进行系统性规制的行政法规,《条例》不再将此类活动仅视为科研探索,而是将其纳入严格的行政许可与合规监管框架,为行业的健康有序发展设定了清晰的“交通规则”。
对于医疗机构、生物科技企业及广大研发者而言,《条例》既是一部必须严格遵守的“合规法典”,也是一张指引创新成果安全、合法走向市场的“导航图”。它终结了过往部分领域“无法可依”或“多头管理”的模糊状态,构建了一个以“风险防控”和“伦理审查”为基石,覆盖临床研究备案、研究实施、转化应用审批、上市后监管直至法律责任追究的全生命周期监管体系。该体系与现行《生物安全法》、《药品管理法》、《干细胞临床研究管理办法》、《涉及人的生命科学和医学研究伦理审查办法》等法律法规共同编织成一张严密的法网,任何置身其中的主体都无法回避。
本解读将从医药法律实务者的视角出发,对《条例》进行逐条的精要分析与深度剖析。我们不仅关注条文的字面含义,更致力于揭示其背后的立法意图、潜在的法律风险、与既有法规的衔接与冲突,并为机构与企业提供具前瞻性、可操作的合规指引与战略建议。
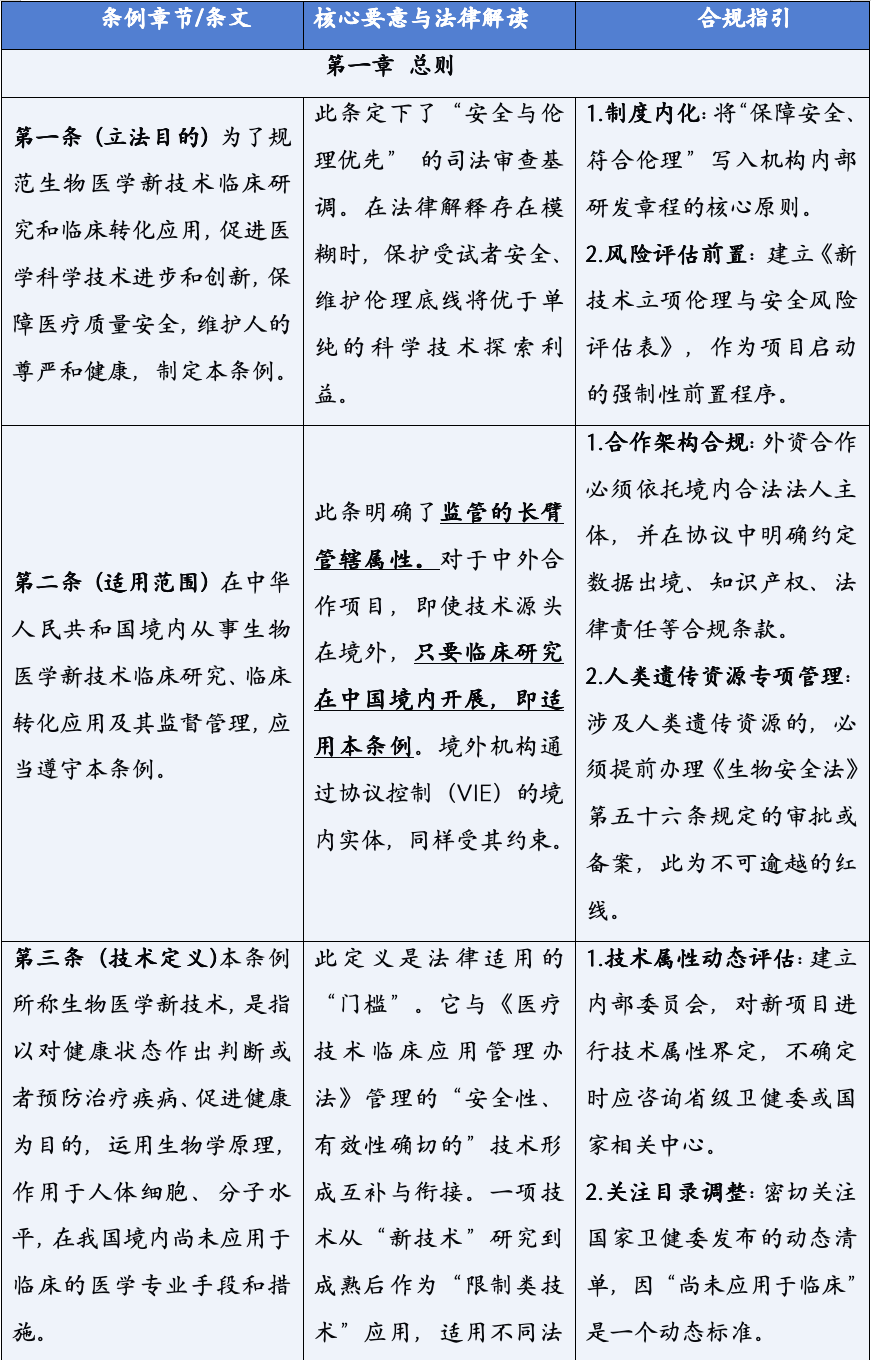
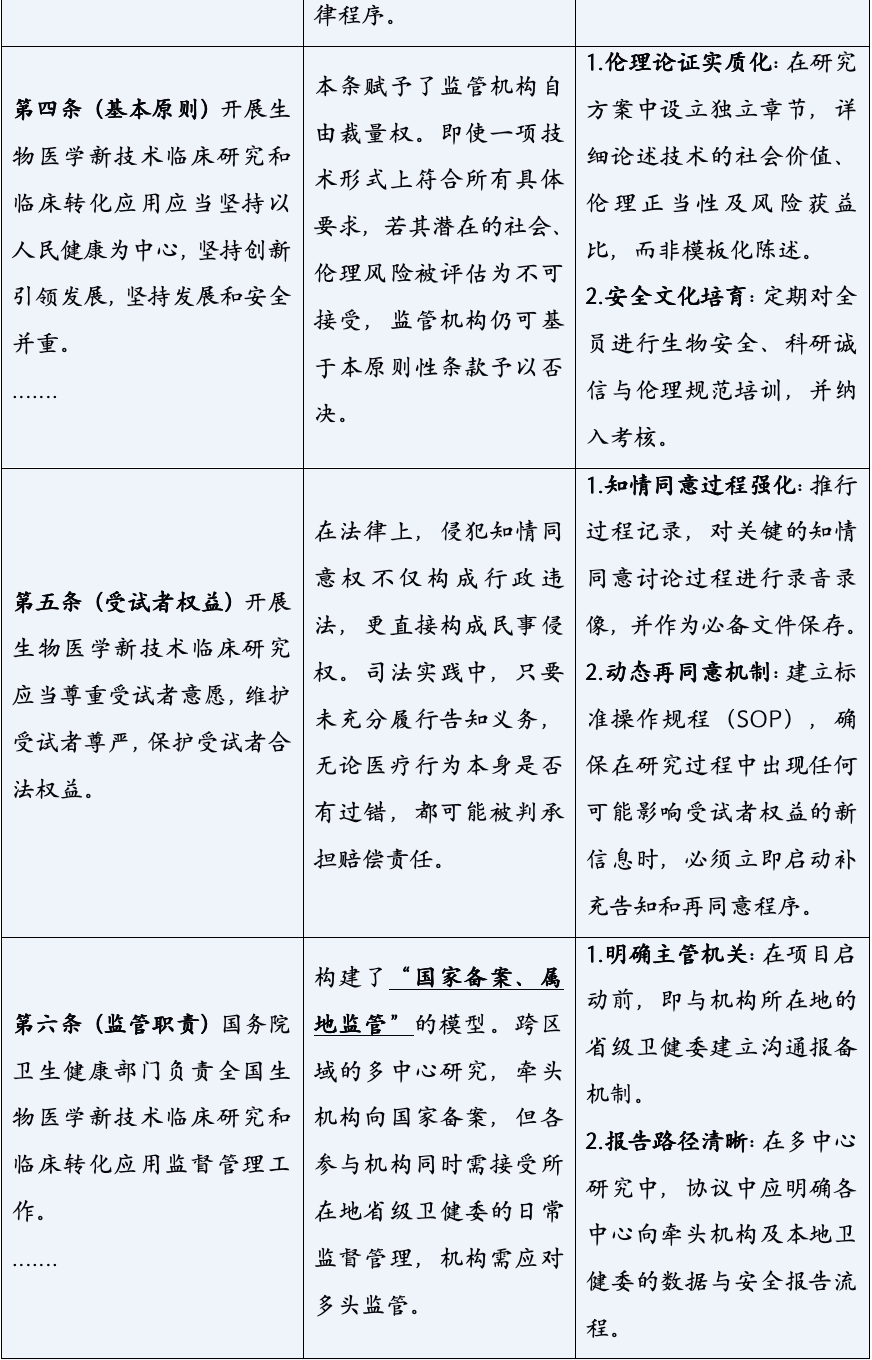
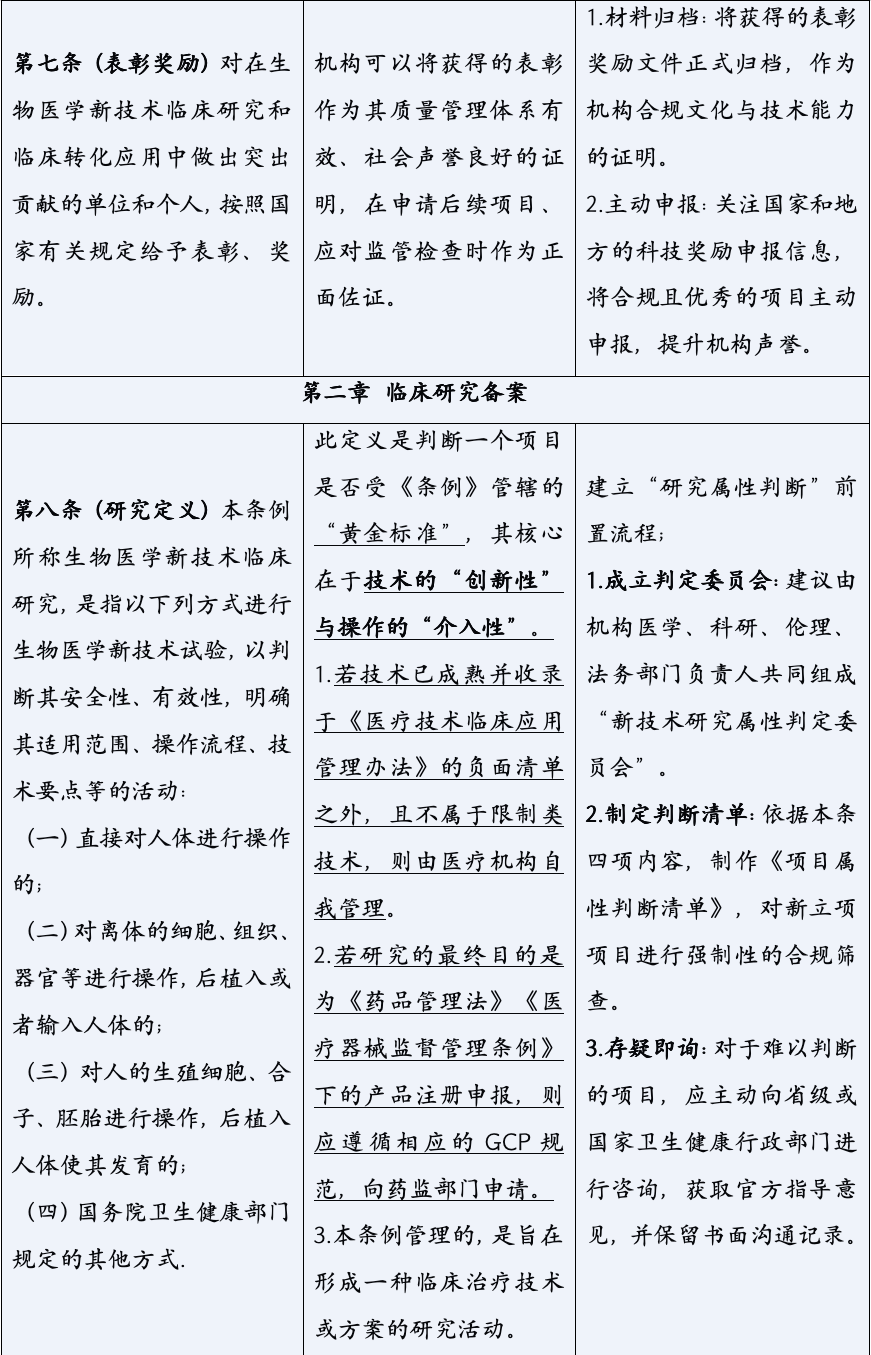

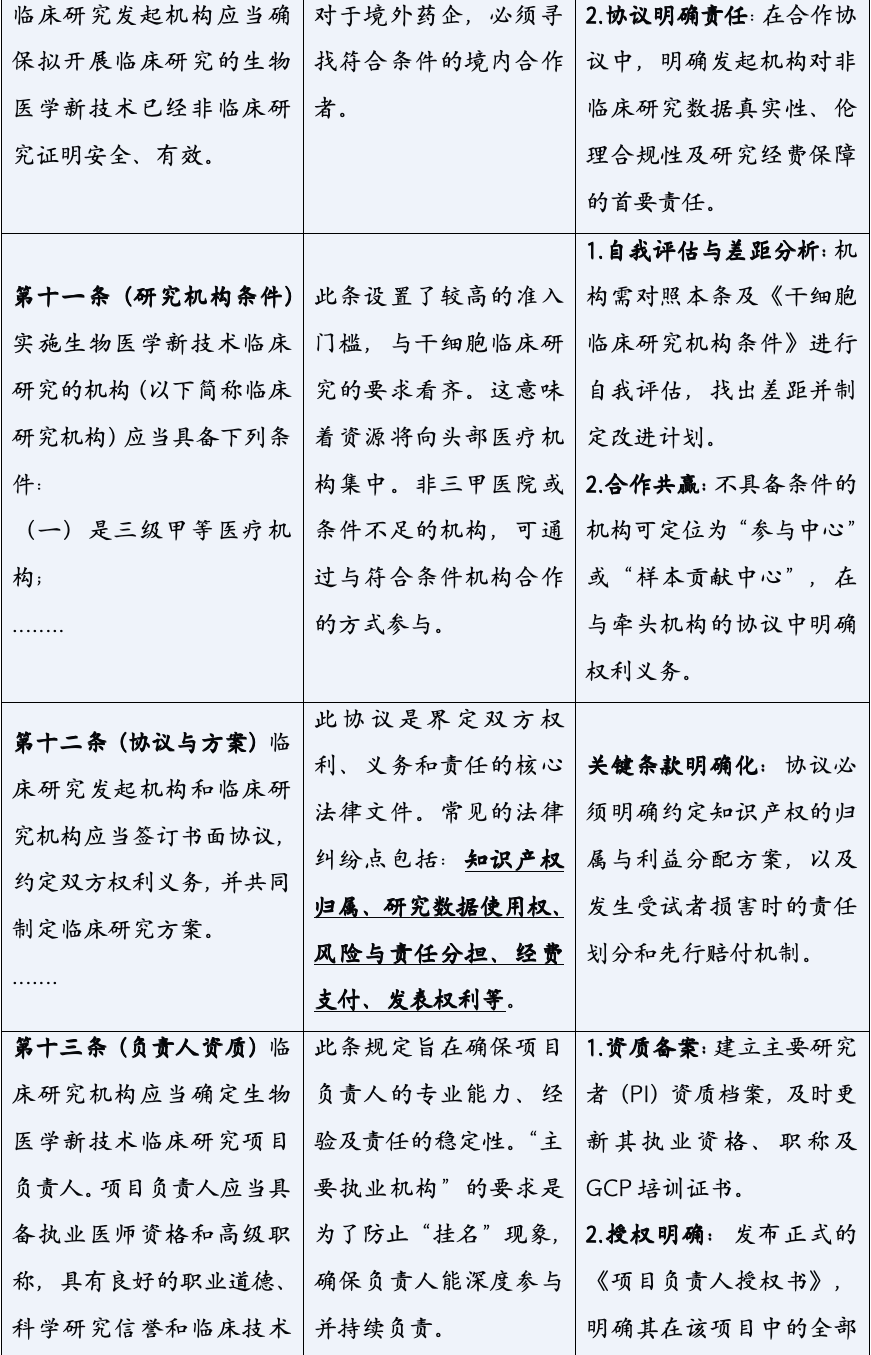
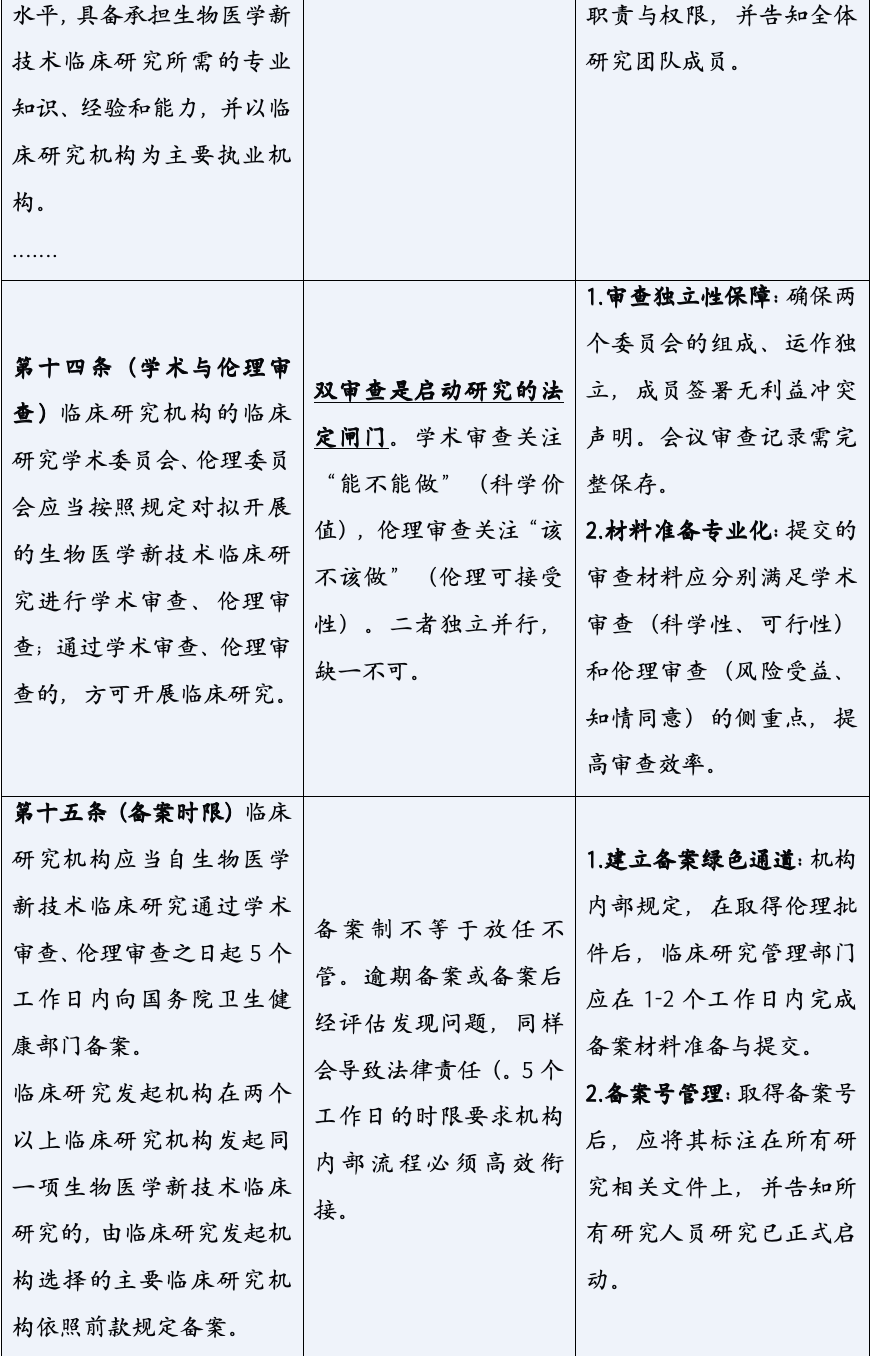
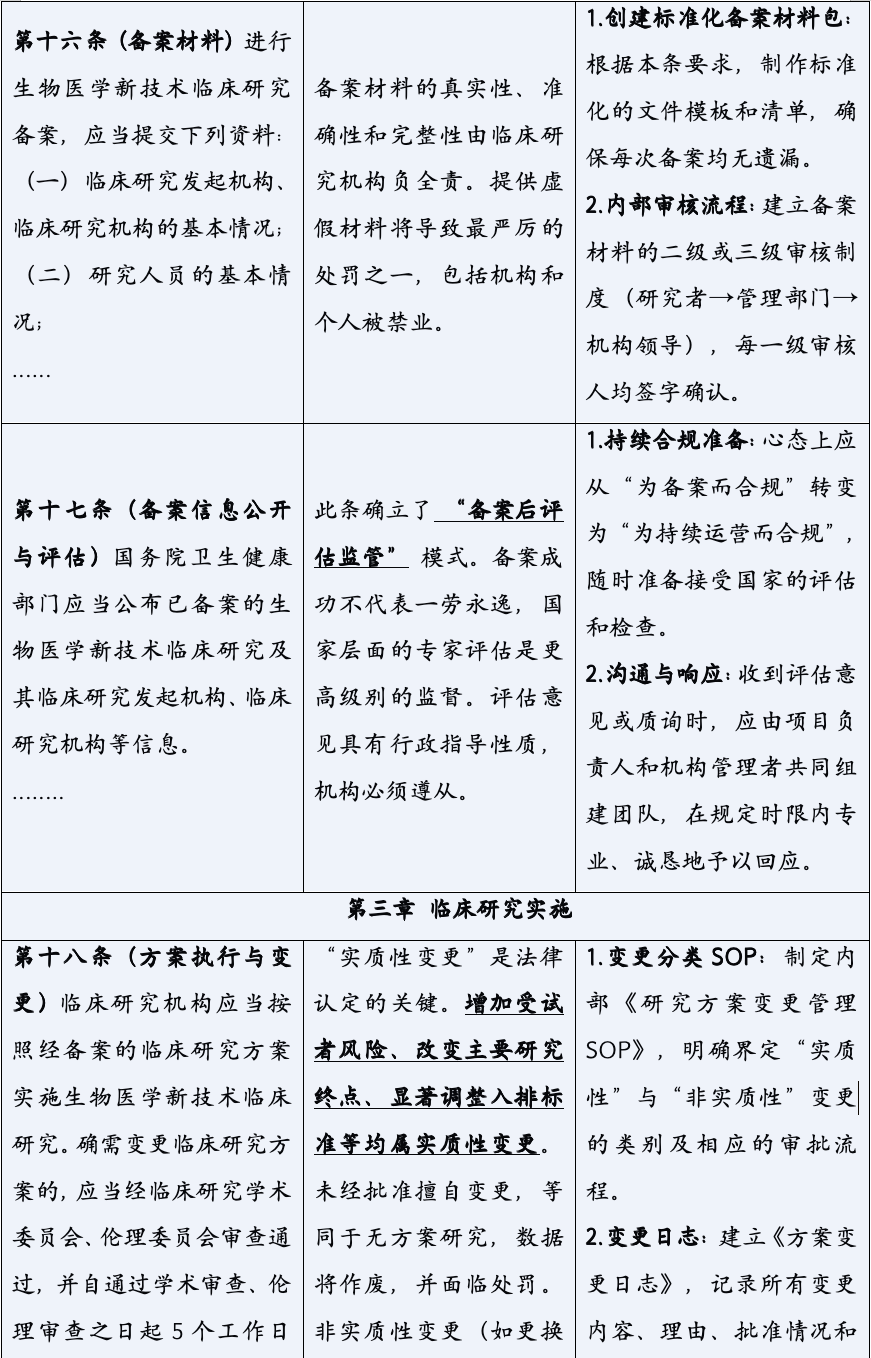
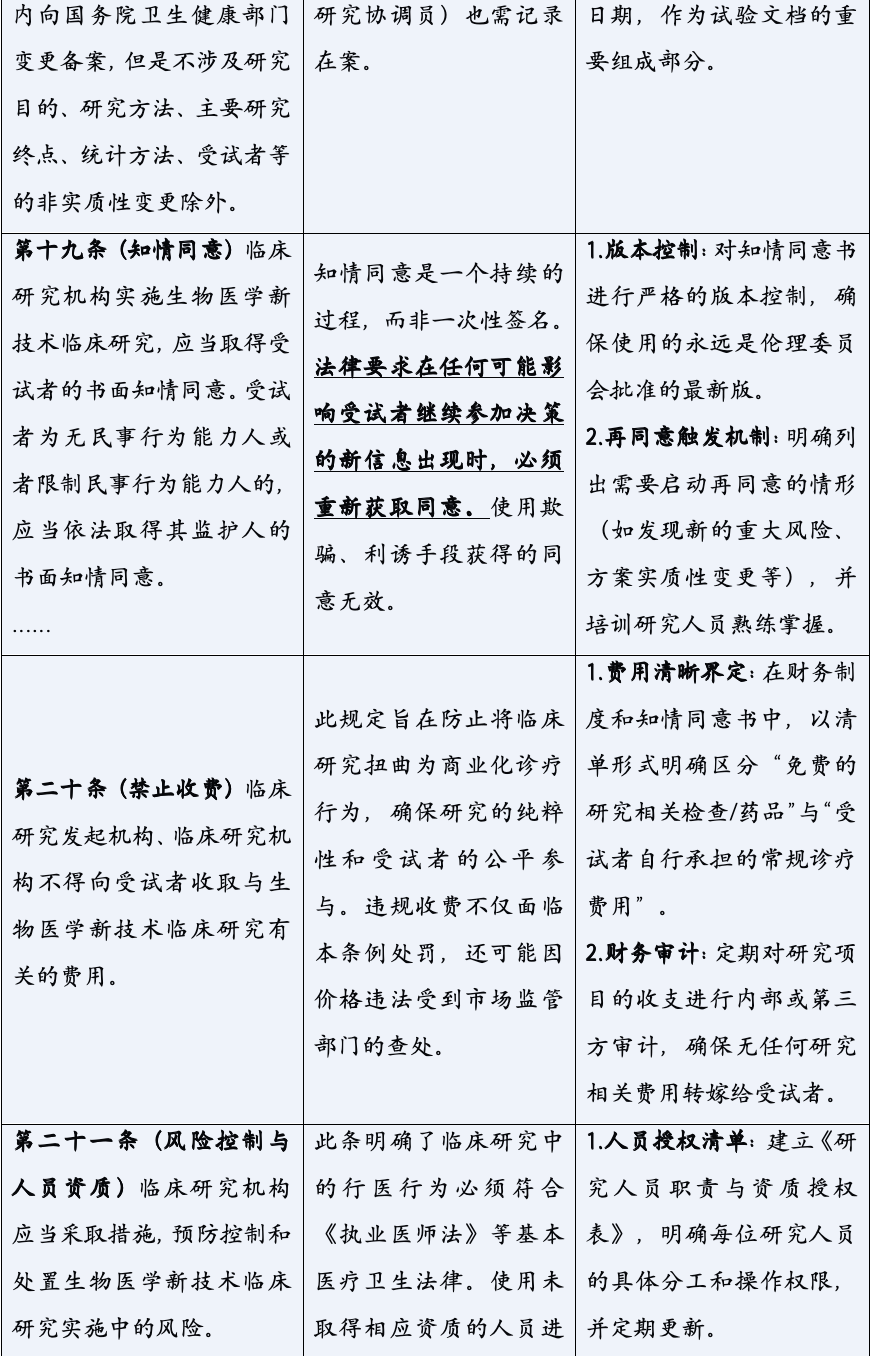
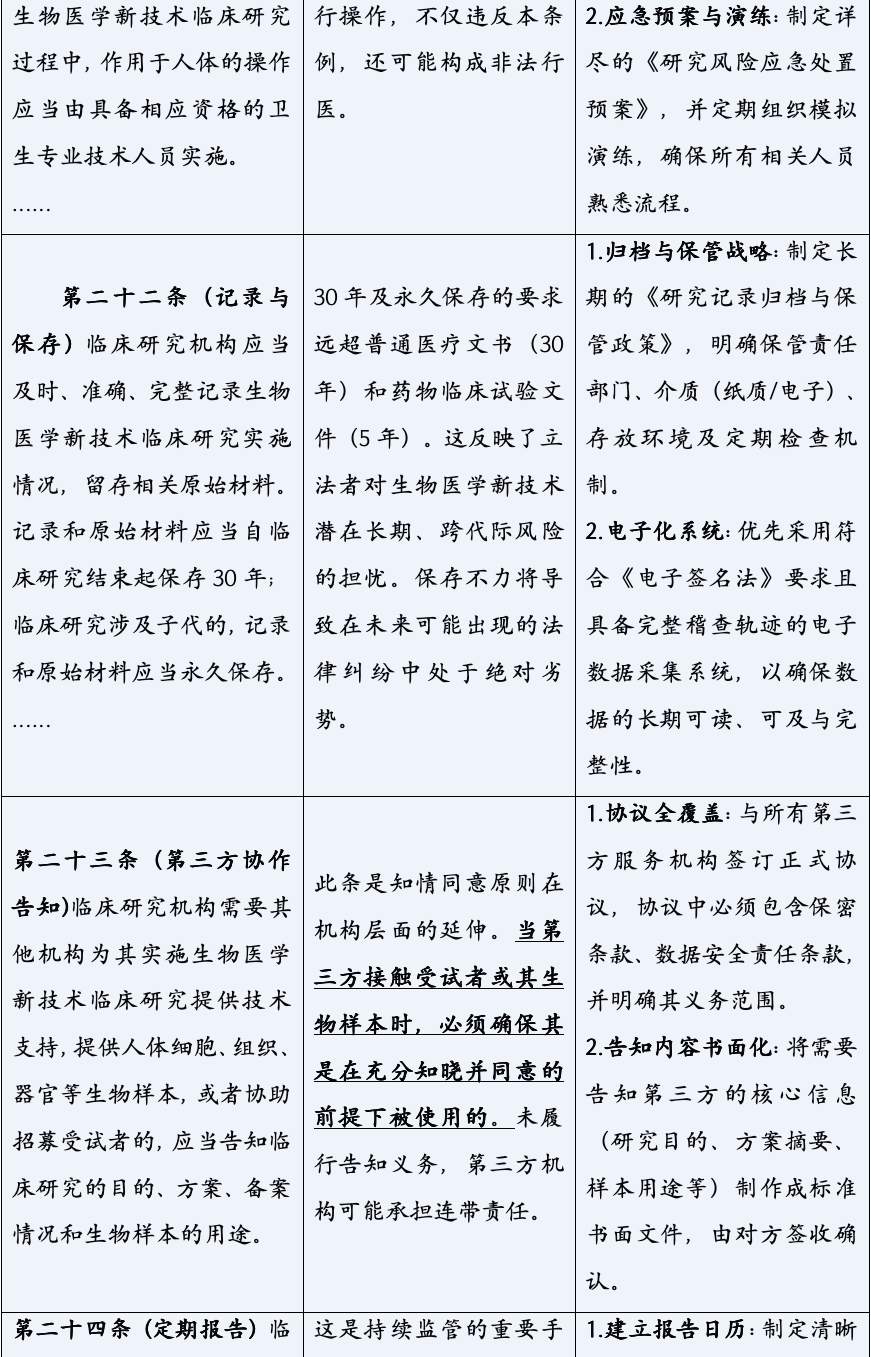
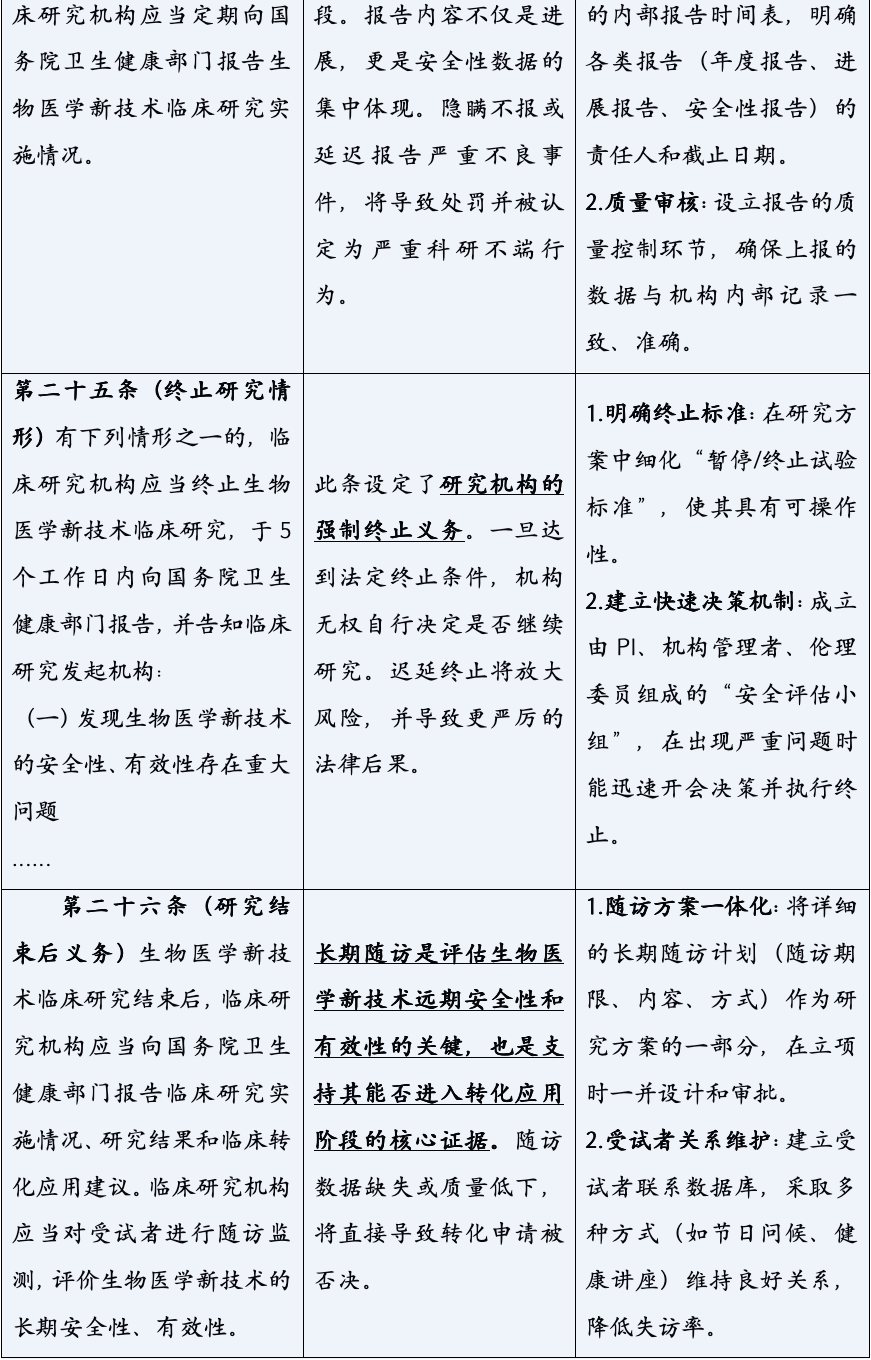
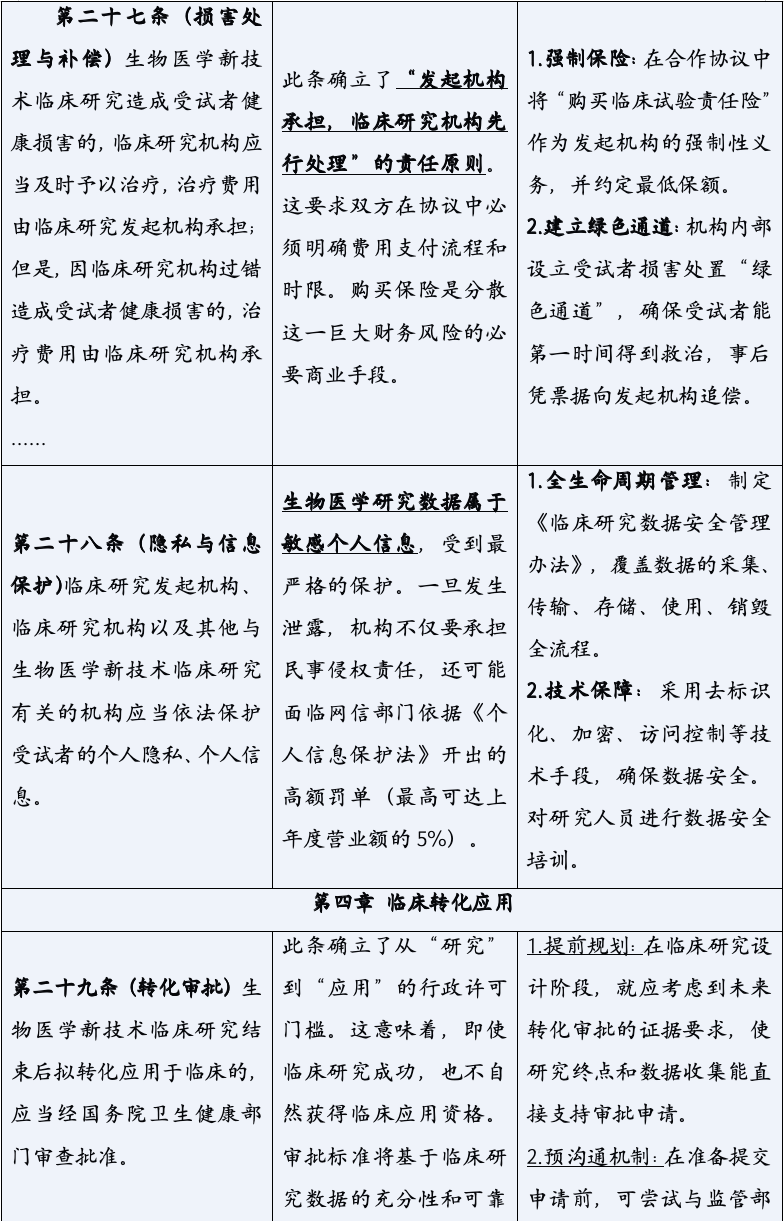
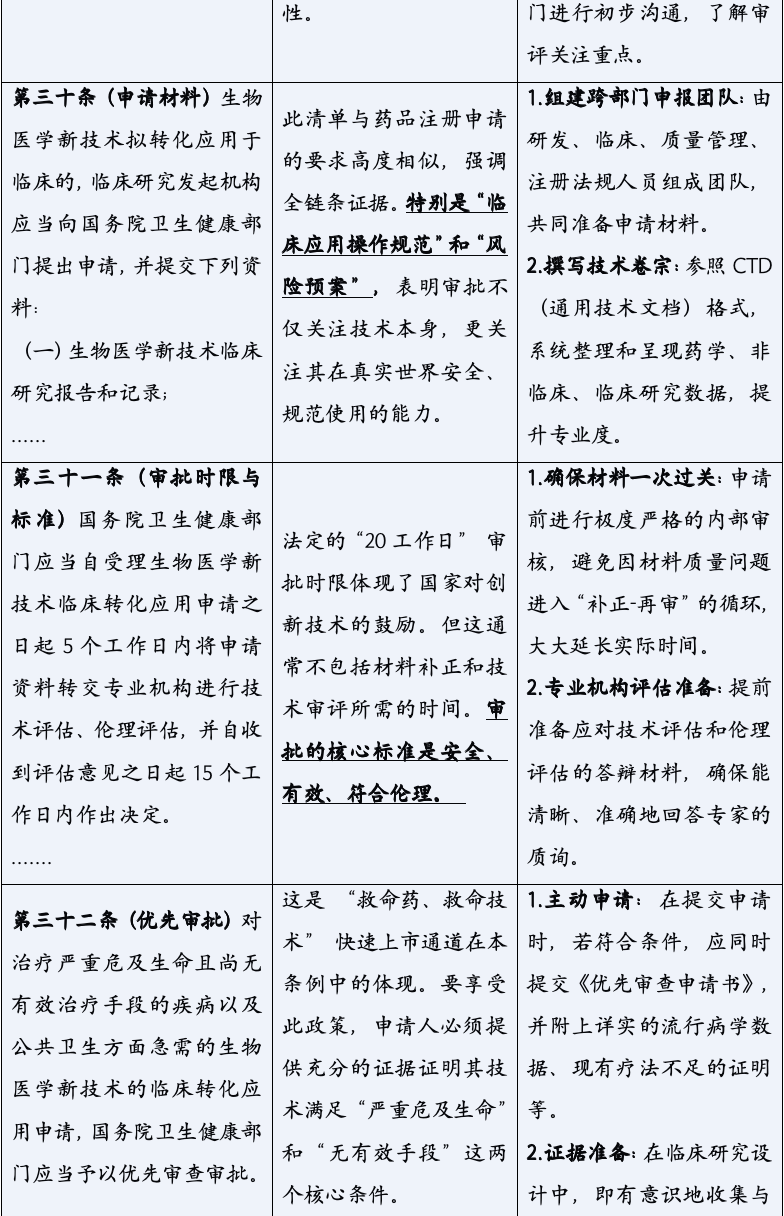
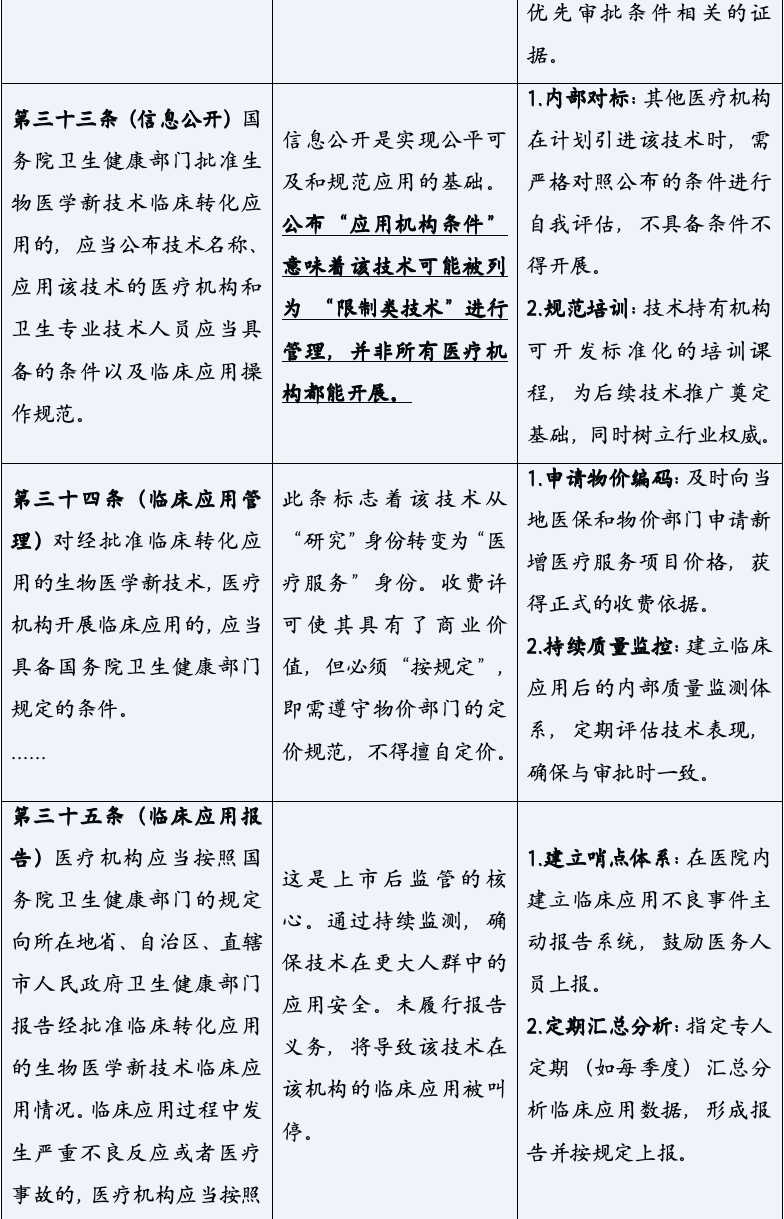
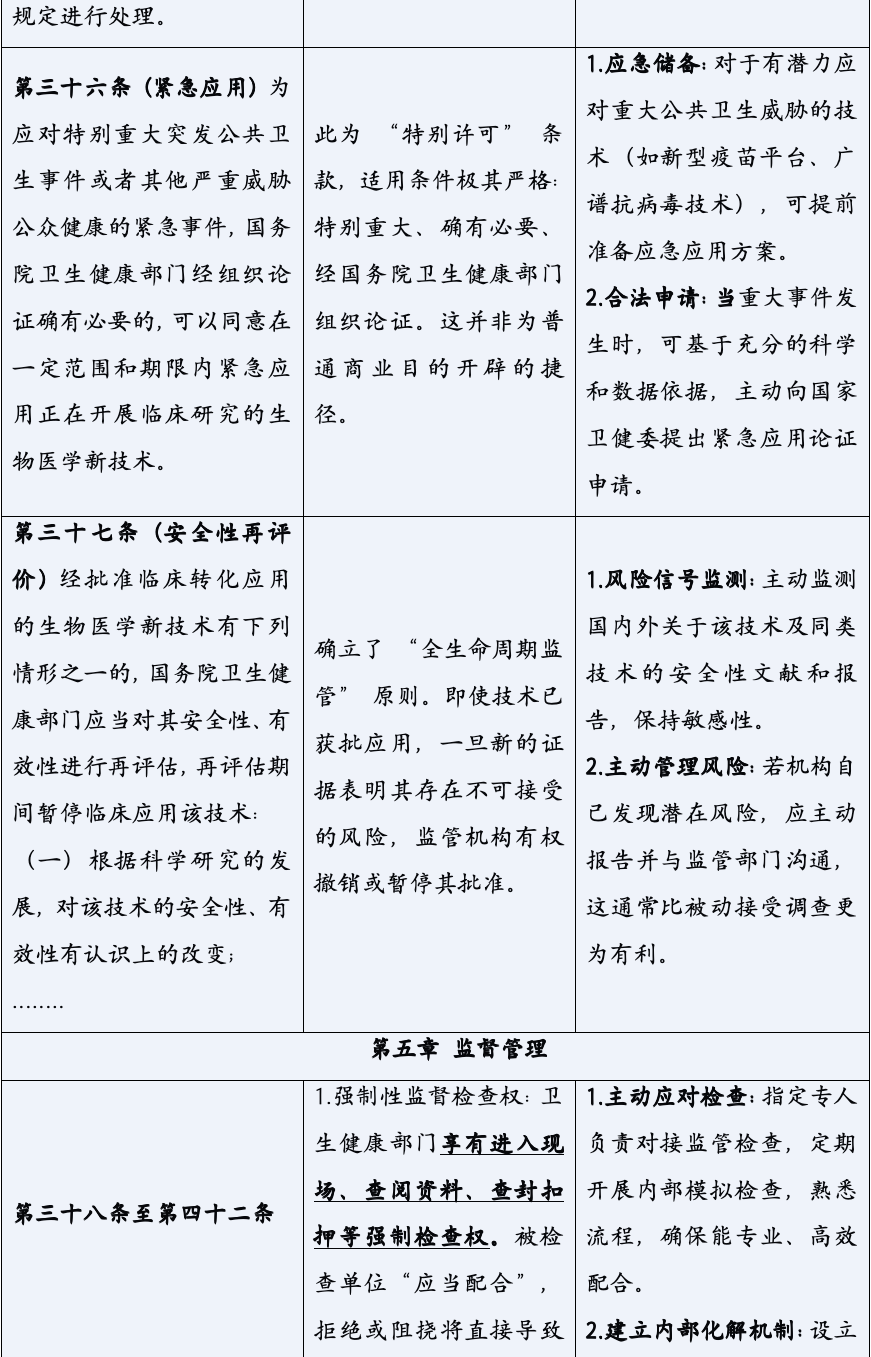
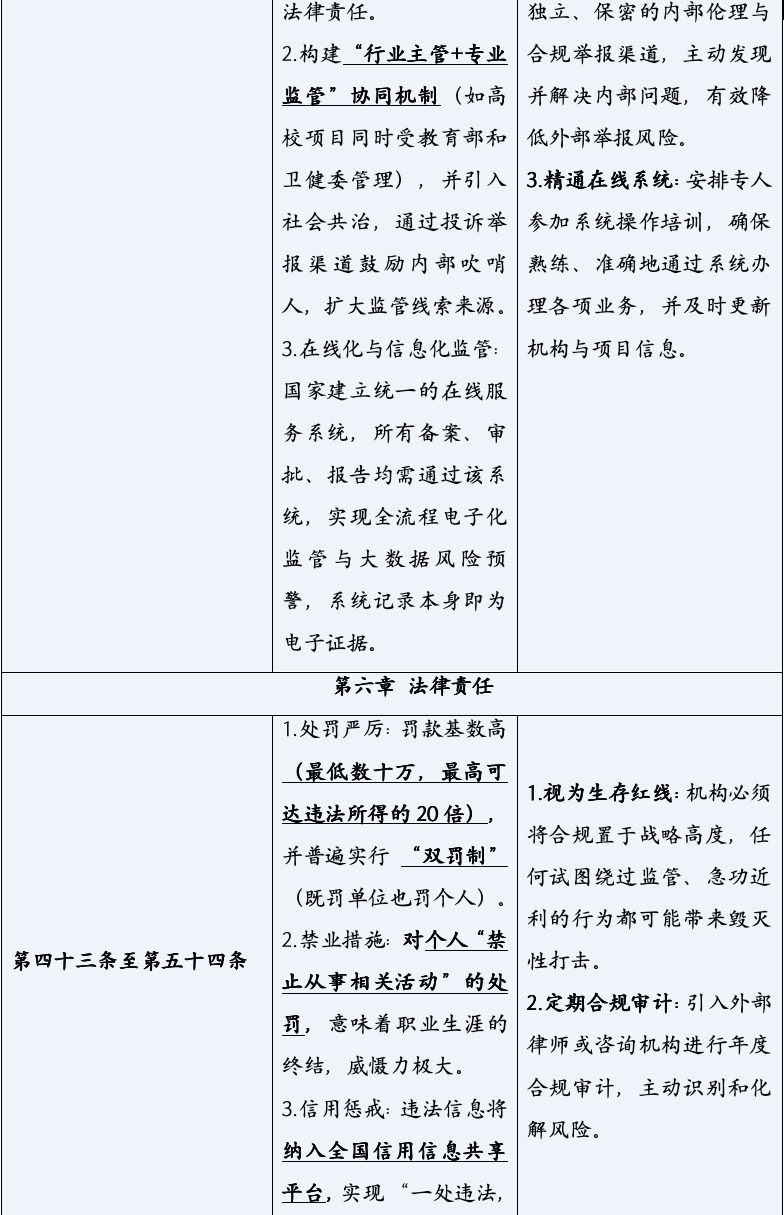
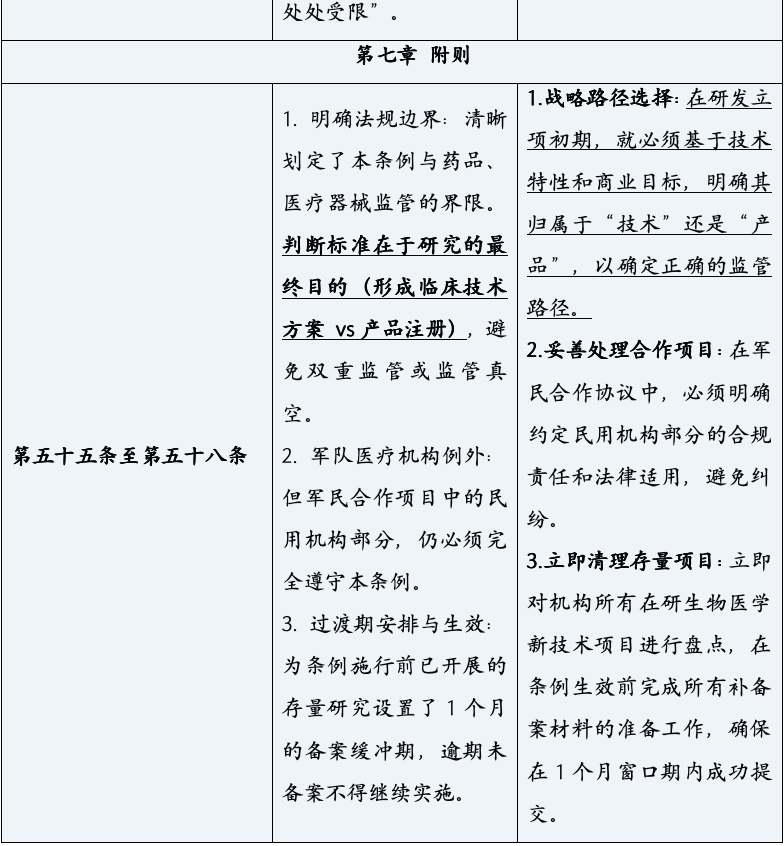
《生物医学新技术临床研究和临床转化应用管理条例》的颁布,标志着中国生物医学领域告别了“野蛮生长”的时代,步入了一个法治化、规范化发展的新纪元。它以其全面系统的监管框架、严格明确的法律责任,为行业的未来划定了清晰的赛道与边界。对于所有参与者而言,深入理解并主动适应这一新规,已不再是应对监管的被动选择,而是决定创新能否实现其科学价值与社会价值,乃至机构能否在激烈竞争中行稳致远的核心战略能力。合规,不再是束缚创新的成本,而是保障创新安全、高效转化的基石,是最核心的竞争力之一。
作者简介

姚琴律师
本科毕业于西南医科大学、研究生毕业于北京理工大学,现为北京市东卫律师事务所执业律师,北京市多家三甲医院伦理委员会委员、《中国医学伦理学》杂志质量提升委员会委员。曾就职于国内知名三甲医院从事医政医务管理工作;加入律师行业后,主要从事医药医疗类法律业务,曾担任多家医药、医疗集团、医生集团、医疗类科技公司等的法律顾问;办理过国内知名生物制药企业、医药流通企业合规体系建设业务;多家非公立医疗机构的并购业务,对医药医疗企业的运营模式,合规问题有丰富的行业经验和实操技能。


